Dược lý và Lâm sàng của Sugammadex: Tích hợp dữ liệu từ Clinical Anesthesia Ấn bản Thứ 10 năm 2025.
Sự ra đời của sugammadex đã đánh dấu một bước ngoặt mang tính cách mạng trong chuyên ngành gây mê hồi sức, thay đổi hoàn toàn cách tiếp cận đối với việc hóa giải phong bế thần kinh cơ. Trong nhiều thập kỷ, các bác sĩ gây mê phải đối mặt với những hạn chế cố hữu của các thuốc kháng cholinesterase như neostigmine, vốn hoạt động gián tiếp và gây ra hàng loạt tác dụng phụ cholinergic không mong muốn. Dựa trên những cập nhật mới nhất từ tài liệu Clinical Anesthesia ấn bản lần thứ 10 năm 2025, báo cáo này sẽ phân tích chi tiết từ nền tảng dược lý phân tử đến các ứng dụng lâm sàng phức tạp của sugammadex, một chất gắn kết giãn cơ chọn lọc (SRBA) đầu tiên trong nhóm.
Nền tảng Dược lý Phân tử và Cơ chế Bao vây đặc hiệu
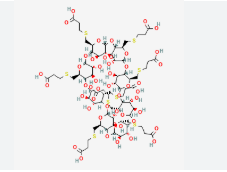
Sugammadex là một gamma-cyclodextrin đã được sửa đổi về mặt cấu trúc, được thiết kế đặc biệt để tạo thành một phức hợp bao vây bền vững với các thuốc giãn cơ steroid không khử cực, chủ yếu là rocuronium và vecuronium. Cyclodextrin là những oligosaccharide vòng được tạo thành từ các đơn vị glucose liên kết với nhau bằng liên kết alpha-1,4-glycosid. Trong khi alpha và beta-cyclodextrin có khoang trung tâm nhỏ, gamma-cyclodextrin với tám đơn vị glucose cung cấp một khoang đủ lớn để chứa các phân tử lớn hơn như thuốc giãn cơ steroid.
Cấu trúc hình học của sugammadex giống như một hình nón cụt hoặc hình bánh vòng, với khoang bên trong có tính kỵ nước (lipophilic) và bề mặt bên ngoài có tính ưa nước (hydrophilic). Sự đổi mới quan trọng trong thiết kế của sugammadex là việc bổ sung tám nhóm carboxyl ở các đầu của chuỗi bên. Các nhóm carboxyl mang điện tích âm này không chỉ giúp duy trì cấu trúc mở của khoang thông qua lực đẩy tĩnh điện mà còn tạo ra lực hút đối với các nhóm amoni bậc bốn mang điện tích dương trên phân tử rocuronium hoặc vecuronium.
Cơ chế hoạt động của sugammadex không dựa trên sự cạnh tranh tại thụ thể nicotinic acetylcholine ở bản vận động thần kinh cơ. Thay vào đó, nó hoạt động bằng cách bao vây trực tiếp phân tử thuốc giãn cơ trong huyết tương theo tỷ lệ mol 1:1. Khi được tiêm vào tĩnh mạch, sugammadex nhanh chóng bao vây các phân tử rocuronium tự do trong huyết tương, làm giảm nồng độ thuốc giãn cơ tự do một cách đột ngột. Điều này thiết lập một gradient nồng độ, thúc đẩy các phân tử rocuronium đang gắn tại các thụ thể acetylcholine ở khe synap khuếch tán ngược trở lại vào huyết tương để đạt được trạng thái cân bằng mới. Tại đây, chúng ngay lập tức bị sugammadex bao vây và làm mất hoạt tính.
Độ bền của phức hợp sugammadex-rocuronium là cực kỳ cao, được duy trì bởi lực van der Waals, tương tác kỵ nước và liên kết hydro. Hằng số liên kết (Ka) được ước tính vào khoảng 10^7 M^-1, nghĩa là phức hợp này cực kỳ ổn định và tỷ lệ phân ly là rất thấp (khoảng 1 trên 25 triệu phức hợp). Sự ổn định này đảm bảo rằng một khi thuốc giãn cơ đã bị bao vây, nó sẽ không thể tái gắn kết vào thụ thể, từ đó loại bỏ nguy cơ tái giãn cơ (recurarization) nếu liều lượng được tính toán chính xác.
| Đặc tính phân tử | Chi tiết thông số |
| Trọng lượng phân tử | 2,178 Daltons |
| Đường kính khoang trung tâm | 7.5 – 8.3 Å |
| Độ hòa tan trong nước | Rất cao |
| Tỷ lệ gắn kết | 1:1 (molar) |
| Ái lực ưu tiên | Rocuronium > Vecuronium >> Pancuronium |
| pH dung dịch | ~ 7.5 |
Dược động học và Quá trình Thải trừ trong các Điều kiện Sinh lý
Sugammadex thể hiện các đặc tính dược động học tuyến tính trong phạm vi liều từ 1 mg/kg đến 16 mg/kg. Sau khi tiêm tĩnh mạch, thể tích phân bố ở trạng thái ổn định vào khoảng 11 đến 14 lít ở người lớn có chức năng thận bình thường, cho thấy thuốc phân bố chủ yếu trong huyết tương và dịch ngoại bào. Do trọng lượng phân tử lớn và tính ưa nước cao, sugammadex không dễ dàng xuyên qua hàng rào máu não hoặc các màng tế bào.
Một đặc điểm dược lý quan trọng là sugammadex không bị chuyển hóa trong cơ thể. Thuốc được thải trừ gần như hoàn toàn (khoảng 90%) dưới dạng không đổi qua nước tiểu trong vòng 24 giờ thông qua quá trình lọc tại cầu thận. Thời gian bán thải trung bình ở người trưởng thành khỏe mạnh là khoảng 2 giờ, với độ thanh thải huyết tương xấp xỉ 88 mL/phút.
Sự phụ thuộc hoàn toàn vào thận để thải trừ cả sugammadex tự do và phức hợp sugammadex-rocuronium đặt ra những cân nhắc quan trọng đối với bệnh nhân suy thận. Mặc dù khả năng bao vây của sugammadex không bị ảnh hưởng bởi chức năng thận, thời gian lưu lại của phức hợp trong tuần hoàn sẽ kéo dài đáng kể khi độ thanh thải creatinine giảm. Ở bệnh nhân suy thận nặng (CrCl < 30 mL/min), thời gian bán thải có thể kéo dài lên tới 19 giờ hoặc hơn. Tuy nhiên, các nghiên cứu cho thấy phức hợp này vẫn duy trì sự ổn định lâu dài trong huyết tương và có thể được loại bỏ hiệu quả thông qua lọc máu bằng màng lọc hiệu suất cao.
| Thông số dược động học | Giá trị ở người lớn bình thường |
| Thời gian bán thải (t1/2) | ~ 2 giờ |
| Độ thanh thải huyết tương | ~ 88 mL/phút |
| Thể tích phân bố (V_dss) | 11 – 14 Lít |
| Liên kết protein huyết tương | Tối thiểu |
| Chuyển hóa | Không đáng kể |
| Bài tiết | Thận (90% trong 24h) |
Chiến lược Liều lượng và Vai trò của Theo dõi Thần kinh cơ Định lượng
Dữ liệu từ Clinical Anesthesia 10th Edition 2025 nhấn mạnh rằng liều lượng sugammadex phải được điều chỉnh dựa trên độ sâu của phong bế thần kinh cơ tại thời điểm hóa giải, được xác định bằng các phương pháp kích thích dây thần kinh ngoại vi. Việc sử dụng liều cố định mà không theo dõi thần kinh cơ có thể dẫn đến việc hóa giải không hoàn toàn hoặc lãng phí tài nguyên y tế.
Hóa giải phong bế mức độ trung bình
Phong bế mức độ trung bình được xác định khi có sự xuất hiện trở lại của đáp ứng thứ hai (T2) trong chuỗi bốn (Train-of-Four – TOF). Liều khuyến cáo trong trường hợp này là 2 mg/kg trọng lượng cơ thể thực tế. Với liều lượng này, thời gian phục hồi tỷ số TOF lên mức ≥ 0.9 thường chỉ mất khoảng 2 đến 3 phút. Đây là một sự cải thiện đáng kể so với neostigmine, vốn yêu cầu thời gian lâu hơn và có độ biến thiên lớn về khả năng phục hồi hoàn toàn.
Hóa giải phong bế mức độ sâu
Phong bế sâu được định nghĩa là khi không có đáp ứng TOF (TOF = 0) nhưng có ít nhất 1-2 đáp ứng sau kích thích tetanic (Post-Tetanic Count – PTC). Liều khuyến cáo để hóa giải phong bế ở độ sâu này là 4 mg/kg. Thời gian phục hồi trung bình đạt tỷ số TOF ≥ 0.9 là khoảng 3 đến 4 phút. Khả năng hóa giải nhanh chóng từ mức độ phong bế sâu là một ưu thế độc nhất của sugammadex, cho phép duy trì điều kiện phẫu thuật tối ưu cho đến tận những giây phút cuối cùng của ca mổ, đặc biệt quan trọng trong phẫu thuật nội soi và robot.
Hóa giải tức thì (Tình huống khẩn cấp)
Trong các tình huống “không thể đặt nội khí quản, không thể thông khí” (CICV) xảy ra ngay sau khi tiêm một liều cao rocuronium (ví dụ 1.2 mg/kg để khởi mê nhanh), liều sugammadex 16 mg/kg được khuyến cáo để hóa giải tức thì. Liều này có thể được sử dụng sớm nhất là 3 phút sau khi tiêm rocuronium và cho thấy khả năng phục hồi nhịp thở tự nhiên nhanh hơn so với sự phục hồi tự nhiên sau khi dùng succinylcholine. Tuy nhiên, cần lưu ý rằng liều 16 mg/kg chỉ được nghiên cứu và phê duyệt để hóa giải rocuronium, chưa có đủ dữ liệu an toàn cho vecuronium ở mức liều này.
| Mức độ phong bế | Tiêu chuẩn theo dõi (NMT) | Liều Sugammadex khuyến cáo |
| Trung bình | Tái xuất hiện T2 (TOF) | 2 mg/kg |
| Sâu | PTC 1–2; TOF = 0 | 4 mg/kg |
| Tức thì | 3 phút sau liều Rocuronium 1.2 mg/kg | 16 mg/kg |
Sự khác biệt giữa việc sử dụng liều khuyến cáo của nhà sản xuất so với việc chuẩn độ liều đã được nghiên cứu kỹ lưỡng. Một nghiên cứu so sánh cho thấy việc chuẩn độ sugammadex theo các bước 50 mg có thể giúp giảm tổng liều sử dụng nhưng lại làm kéo dài thời gian để đạt được tỷ số TOF ≥ 0.9 so với việc sử dụng liều bolus duy nhất theo khuyến cáo. Do đó, trong thực hành lâm sàng tiêu chuẩn, việc sử dụng liều bolus dựa trên trọng lượng cơ thể thực tế vẫn được ưu tiên để đảm bảo tính dự đoán và tốc độ phục hồi.
Hiệu quả Lâm sàng và Cải thiện Kết cục Hậu phẫu
Lợi ích của sugammadex không chỉ dừng lại ở tốc độ hóa giải mà còn mở rộng sang việc cải thiện độ an toàn cho bệnh nhân trong giai đoạn hồi tỉnh. Một trong những vấn đề nghiêm trọng nhất trong gây mê hiện đại là tình trạng liệt tồn dư sau mổ (Residual Neuromuscular Blockade – RNMB), được định nghĩa là tỷ số TOF < 0.9 khi bệnh nhân rời phòng mổ.
Các thuốc hóa giải truyền thống như neostigmine có “hiệu ứng trần” (ceiling effect), nghĩa là khi nồng độ acetylcholine tại khe synap đạt mức tối đa do sự ức chế hoàn toàn acetylcholinesterase, việc tăng thêm liều neostigmine không mang lại hiệu quả hóa giải mạnh hơn. Điều này dẫn đến tỷ lệ liệt tồn dư cao, từ 30% đến 60%, liên quan trực tiếp đến các biến chứng hô hấp hậu phẫu như giảm oxy máu, xẹp phổi và viêm phổi do hít. Ngược lại, sugammadex thông qua cơ chế bao vây trực tiếp có thể loại bỏ hoàn toàn thuốc giãn cơ khỏi thụ thể, làm giảm tỷ lệ RNMB xuống gần như bằng không khi được sử dụng đúng liều lượng.
Hơn nữa, sugammadex không có tác dụng phụ cholinergic, do đó không cần sử dụng đồng thời các thuốc kháng muscarinic như atropine hay glycopyrrolate. Điều này giúp tránh được các biến chứng như nhịp tim nhanh, khô miệng, bí tiểu và mê sảng hậu phẫu, đặc biệt có lợi cho bệnh nhân cao tuổi hoặc bệnh nhân có bệnh lý tim mạch đi kèm.
Trong phẫu thuật nhãn khoa, sugammadex cho thấy ưu thế vượt trội khi làm giảm đáng kể áp lực nội nhãn (IOP) tại thời điểm rút nội khí quản so với sự kết hợp neostigmine-atropine. Việc kiểm soát IOP ổn định là yếu tố then chốt cho sự thành công của các ca mổ mắt xuyên thấu hoặc bệnh nhân glaucoma. Tương tự, trong các phẫu thuật yêu cầu phong bế sâu liên tục như nội soi ổ bụng áp lực thấp hoặc phẫu thuật robot, sugammadex cho phép bác sĩ gây mê duy trì độ giãn cơ tối ưu cho đến khi đóng da mà không lo ngại về việc kéo dài thời gian hồi tỉnh.
| Chỉ số so sánh | Sugammadex | Neostigmine + Kháng Muscarinic |
| Cơ chế | Bao vây trực tiếp (Scavenging) | Ức chế Enzyme (Cạnh tranh) |
| Tác dụng phụ tim mạch | Nhịp chậm (hiếm gặp) | Nhịp nhanh, loạn nhịp |
| Tác dụng phụ cholinergic | Không có | Tiết dịch, co thắt phế quản |
| Khả năng hóa giải phong bế sâu | Rất tốt | Rất kém / Không thể |
| Nguy cơ liệt tồn dư | Cực thấp | Cao (30–60%) |
| Hiệu quả kinh tế (thời gian OR) | Tiết kiệm thời gian đáng kể | Tốn thêm thời gian chờ đợi |
Quản lý Sugammadex trong các Quần thể Bệnh nhân Đặc biệt
Việc sử dụng sugammadex đòi hỏi sự hiểu biết sâu sắc về các thay đổi sinh lý bệnh ở các nhóm đối tượng cụ thể để đảm bảo an toàn tối đa.
Bệnh nhân Suy thận
Mặc dù sugammadex không bị chuyển hóa và thải trừ qua thận, việc sử dụng ở bệnh nhân có mức lọc cầu thận CrCl < 30 mL/min vẫn là một chủ đề gây tranh luận. FDA hiện tại không khuyến cáo sử dụng sugammadex cho nhóm này do thiếu dữ liệu an toàn dài hạn về việc tích tụ phức hợp sugammadex-rocuronium. Tuy nhiên, các báo cáo lâm sàng và Clinical Anesthesia 10th Edition 2025 chỉ ra rằng trong các tình huống cần thiết, sugammadex vẫn có thể được sử dụng thận trọng. Phức hợp này rất ổn định và không giải phóng rocuronium tự do trở lại máu một cách đáng kể. Đối với bệnh nhân đang lọc máu chu kỳ, việc sử dụng màng lọc high-flux có thể loại bỏ phức hợp một cách hiệu quả.
Trẻ em và Trẻ sơ sinh
Sugammadex đã được phê duyệt cho trẻ em từ 2 tuổi trở lên với liều lượng tương tự như người lớn. Ở nhóm đối tượng này, sugammadex cho thấy hồ sơ an toàn tốt và giúp giảm đáng kể thời gian rút nội khí quản, điều này cực kỳ quan trọng ở trẻ em vốn có dự trữ hô hấp thấp. Đối với trẻ dưới 2 tuổi và trẻ sơ sinh, việc sử dụng vẫn được coi là “off-label”. Mặc dù vậy, các nghiên cứu quy mô nhỏ và báo cáo ca lâm sàng cho thấy trẻ sơ sinh phục hồi rất nhanh sau khi dùng sugammadex liều 2-4 mg/kg, với thời gian phục hồi TOF > 0.9 thường dưới 2 phút. Tuy nhiên, do hệ thống thận của trẻ sơ sinh chưa hoàn thiện, việc theo dõi sát tình trạng tái giãn cơ là bắt buộc.
Bệnh nhân Béo phì
Đối với bệnh nhân béo phì, liều lượng sugammadex phải được tính toán dựa trên trọng lượng cơ thể thực tế (Actual Body Weight – ABW). Việc tính liều theo trọng lượng lý tưởng (Ideal Body Weight – IBW) thường dẫn đến liều lượng không đủ để bao vây toàn bộ lượng thuốc giãn cơ có trong cơ thể, dẫn đến việc phục hồi chậm hoặc liệt tồn dư. Các nghiên cứu đã xác nhận rằng sử dụng ABW mang lại tốc độ phục hồi nhanh chóng và dự đoán được mà không làm tăng đáng kể các tác dụng phụ nghiêm trọng.
Bệnh nhân có bệnh lý thần kinh cơ (Myasthenia Gravis, loạn dưỡng cơ)
Sugammadex là một bước tiến lớn cho bệnh nhân nhược cơ (Myasthenia Gravis) hoặc loạn dưỡng cơ Duchenne. Những bệnh nhân này cực kỳ nhạy cảm với thuốc giãn cơ không khử cực và thường có phản ứng không thể dự đoán với neostigmine (vốn có thể gây ra cơn nhược cơ). Việc sử dụng liều thấp rocuronium kết hợp với hóa giải bằng sugammadex giúp đảm bảo an toàn đường thở tối ưu và phục hồi chức năng hô hấp nhanh chóng, giảm thiểu nguy cơ biến chứng phổi hậu phẫu.
Hồ sơ An toàn, Biến cố bất lợi và Tương tác Thuốc
Mặc dù sugammadex được coi là an toàn hơn so với các thuốc hóa giải truyền thống, bác sĩ lâm sàng cần lưu ý đến một số phản ứng có hại quan trọng đã được báo cáo trong các nghiên cứu hậu mãi.
Nhịp chậm và Biến cố Tim mạch
Một trong những tác dụng phụ nghiêm trọng nhất là nhịp chậm xoang, đôi khi tiến triển thành vô tâm thu, xảy ra trong vòng vài phút sau khi tiêm sugammadex. Cơ chế chính xác vẫn chưa được làm rõ hoàn toàn, nhưng có những báo cáo về sự kéo dài khoảng QT liên quan đến thuốc. Theo dõi điện tâm đồ liên tục là bắt buộc trong giai đoạn hóa giải, và atropine nên được chuẩn bị sẵn sàng để xử trí kịp thời các trường hợp nhịp chậm có triệu chứng.
Phản ứng Quá mẫn và Anaphylaxis
Phản ứng phản vệ với sugammadex là một biến chứng hiếm gặp nhưng có thể đe dọa tính mạng, với tỷ lệ ước tính khoảng 1:2.500 đến 1:20.000 trường hợp. Các triệu chứng thường xuất hiện nhanh chóng, bao gồm ban đỏ, mề đay, hạ huyết áp nặng và co thắt phế quản. Việc chẩn đoán có thể khó khăn do trùng lặp với các thuốc khác được sử dụng trong gây mê (như thuốc kháng sinh hoặc chính thuốc giãn cơ). Xử trí anaphylaxis do sugammadex tuân theo các hướng dẫn chuẩn của ACLS với adrenaline là thuốc lựa chọn hàng đầu.
Tương tác với Thuốc tránh thai đường uống
Sugammadex có khả năng gắn kết với các hormone steroid, bao gồm cả progesterone. Điều này dẫn đến một tương tác thuốc quan trọng: một liều sugammadex có thể làm giảm nồng độ thuốc tránh thai đường uống tương đương với việc quên một liều thuốc hàng ngày. Bệnh nhân cần được tư vấn sử dụng các phương pháp tránh thai bổ sung (như bao cao su) trong vòng 7 ngày sau khi nhận sugammadex. Đây là một khía cạnh quan trọng về mặt pháp lý y khoa mà bác sĩ gây mê cần thực hiện và ghi chép trong hồ sơ bệnh án.
Ảnh hưởng đến Đông máu
Dữ liệu in vitro cho thấy liều cao sugammadex có thể làm kéo dài thời gian đông máu (aPTT và PT/INR) một cách tạm thời (thường dưới 60 phút). Tuy nhiên, các nghiên cứu lâm sàng quy mô lớn trên bệnh nhân phẫu thuật không cho thấy sự gia tăng đáng kể nguy cơ chảy máu trên lâm sàng. Mặc dù vậy, cần thận trọng khi sử dụng cho bệnh nhân có rối loạn đông máu nặng hoặc đang sử dụng thuốc chống đông liều cao.
| Biến cố bất lợi | Tần suất / Đặc điểm | Xử trí khuyến cáo |
| Nhịp chậm xoang | Ít gặp nhưng nghiêm trọng | Atropine, Adrenaline |
| Phản vệ (Anaphylaxis) | Hiếm (1:2.500 – 1:20.000) | Epinephrine, dịch truyền, hỗ trợ hô hấp |
| Hạ huyết áp | Thường gặp (liên quan khởi mê) | Dịch truyền, vận mạch |
| Buồn nôn/Nôn | Thường gặp | Thuốc chống nôn |
| Kéo dài QT | Hiếm gặp | Theo dõi điện tâm đồ |
| Giảm hiệu quả tránh thai | Tương tác dược lực học | Tư vấn tránh thai bổ sung trong 7 ngày |
Tái lập phong bế thần kinh cơ sau khi dùng Sugammadex
Trong trường hợp cần tái lập tình trạng giãn cơ cho một bệnh nhân vừa được hóa giải bằng sugammadex, bác sĩ gây mê cần tuân thủ các mốc thời gian dựa trên dược động học của thuốc để đảm bảo hiệu quả:
-
Nếu cần giãn cơ ngay lập tức (< 5 phút): Lựa chọn ưu tiên là các thuốc giãn cơ không thuộc nhóm steroid như succinylcholine (thuốc khử cực) hoặc cisatracurium (thuốc benzylisoquinoline). Sugammadex không có ái lực với các thuốc này.
-
Thời gian chờ từ 5 phút đến 4 giờ: Có thể sử dụng rocuronium với liều 1.2 mg/kg. Cần lưu ý rằng thời gian khởi phát có thể chậm hơn (lên đến 4 phút) và thời gian duy trì phong bế có thể ngắn hơn so với bình thường do vẫn còn một lượng sugammadex dư thừa trong tuần hoàn.
-
Sau 4 giờ (ở bệnh nhân chức năng thận bình thường): Có thể sử dụng lại liều chuẩn của rocuronium (0.6 mg/kg) hoặc vecuronium (0.1 mg/kg).
-
Bệnh nhân suy thận: Thời gian chờ đợi được khuyến cáo là ít nhất 24 giờ trước khi sử dụng lại liều tiêu chuẩn của các thuốc giãn cơ steroid.
| Thời gian sau liều Sugammadex | Thuốc giãn cơ khuyến cáo | Liều lượng lưu ý |
| Cấp cứu (< 5 phút) | Succinylcholine / Cisatracurium | Liều tiêu chuẩn |
| 5 phút – 4 giờ | Rocuronium | 1.2 mg/kg (Khởi phát chậm) |
| > 4 giờ | Rocuronium / Vecuronium | Liều tiêu chuẩn |
| Suy thận | Chờ > 24 giờ | Thận trọng theo dõi NMT |
Hiệu quả Vận hành và Kinh tế Y tế
Mặc dù chi phí trực tiếp của một lọ sugammadex cao hơn nhiều so với neostigmine, các mô hình kinh tế y tế hiện đại trình bày trong Clinical Anesthesia 10th Edition cho thấy sugammadex có thể mang lại hiệu quả về chi phí khi xét trên tổng thể quá trình điều trị.
Việc giảm thời gian chờ đợi phục hồi thần kinh cơ giúp tiết kiệm trung bình 10-25 phút cho mỗi ca phẫu thuật. Tại các trung tâm phẫu thuật có chi phí vận hành phòng mổ cao (ước tính khoảng 8.60 USD mỗi phút), việc tiết kiệm thời gian này trực tiếp bù đắp chi phí thuốc. Ngoài ra, việc giảm 30% tỷ lệ biến chứng phổi hậu phẫu (PPCs) giúp giảm thời gian nằm viện, giảm tỷ lệ tái nhập viện và giảm nhu cầu chăm sóc tích cực, từ đó mang lại giá trị kinh tế lớn cho hệ thống y tế.
Sugammadex cũng đóng vai trò then chốt trong các chương trình Phục hồi sớm sau phẫu thuật (ERAS), nơi việc rút nội khí quản sớm, vận động sớm và giảm thiểu các tác dụng phụ của thuốc gây mê là những trụ cột quan trọng để tối ưu hóa kết cục cho bệnh nhân.
Kết luận
Sugammadex đã thiết lập một tiêu chuẩn vàng mới trong việc hóa giải phong bế thần kinh cơ, cung cấp khả năng phục hồi nhanh chóng, tiên đoán được và an toàn cho bệnh nhân sử dụng rocuronium hoặc vecuronium. Thông qua cơ chế bao vây phân tử độc đáo, nó giải quyết triệt để những hạn chế của các thuốc kháng cholinesterase truyền thống, đặc biệt là trong việc loại bỏ tình trạng liệt tồn dư sau mổ và các tác dụng phụ cholinergic.
Tuy nhiên, sự tiện lợi của sugammadex không nên dẫn đến sự chủ quan trong thực hành. Việc theo dõi thần kinh cơ định lượng vẫn là yêu cầu bắt buộc để đảm bảo liều lượng chính xác và xác nhận sự phục hồi hoàn toàn trước khi rút nội khí quản. Bác sĩ gây mê cần duy trì sự cảnh giác đối với các biến cố hiếm gặp như nhịp chậm và phản vệ, đồng thời thực hiện đầy đủ trách nhiệm tư vấn về tương tác thuốc tránh thai. Với sự hiểu biết sâu sắc về dược lý và lâm sàng theo cập nhật mới nhất năm 2025, sugammadex tiếp tục là một công cụ mạnh mẽ giúp nâng cao chất lượng chăm sóc và an toàn cho bệnh nhân phẫu thuật trên toàn cầu.
TÀI LIỆU THAM KHẢO
MINH HÙNG. NGUYỄN